Grüße die Bewohner unserer Website!
Von Jahr zu Jahr wird die Ölförderung immer komplexer und der daraus gewonnene Kraftstoff wird immer teurer. In den EU-Ländern drohen sie generell, die Produktion von Benzinmotoren einzustellen, sie wollen alle Fahrzeuge durch Elektroautos ersetzen. Aber Lithiumbatterien sind immer noch alles andere als ideal, und sie haben es übrigens nicht eilig, überhaupt ideal zu werden. Im besten Fall kann mit einer einzelnen Ladung eines Lithium-Akkus eine Entfernung von maximal 700 km zurückgelegt werden. Danach müssen Sie den Akku etwa eine Woche lang aufladen. Wenn Sie zum Laden eine normale Steckdose verwenden, dauert dies im Allgemeinen sehr lange. Und Sie stellen sich vor, was passieren wird, wenn jeder anfängt, seine Elektroautos ständig aufzuladen, wie groß die Belastung des Stromnetzes ist und wie viel Spannung abfließt. Im Allgemeinen ist die Zukunft von Lithiumbatterien noch recht vage, und jedes Jahr wird mehr und mehr nach neuen Batterieoptionen gesucht.
Wie Sie wissen, ist Aluminium das energieintensivste Metall. Bereits in unserer Zeit können einige Prototypen von Aluminiumbatterien etwa 2000 km ohne Aufladen fahren, und das Aufladen dieses Batterietyps dauert nur 15 Minuten. Danach können Sie etwa 2000 km weiter fahren.
Das Aufladen von Aluminiumbatterien unterscheidet sich vom Aufladen von Lithiumbatterien. Trotzdem ist nichts kompliziertes daran, Sie müssen nur ein neues Aluminium einsetzen, den Elektrolyten ausschütten und einen neuen Elektrolyten einfüllen, alles ist im Wesentlichen dasselbe wie bei Benzin ein Auto, nur dies ist ein Elektroauto, und das Stromnetz ist nicht belastet. Darüber hinaus müssen Sie keine große Anzahl von Steckdosen mit Drähten mit großem Querschnitt herstellen, um alle diese Elektroautos aufzuladen.
Aber hier ist nicht alles so glatt. Strom aus Aluminium zu bekommen ist gar nicht so einfach, wie wir es uns wünschen. Lassen Sie uns zunächst herausfinden, was das Prinzip der Aluminium-Luft-Batterie ist.
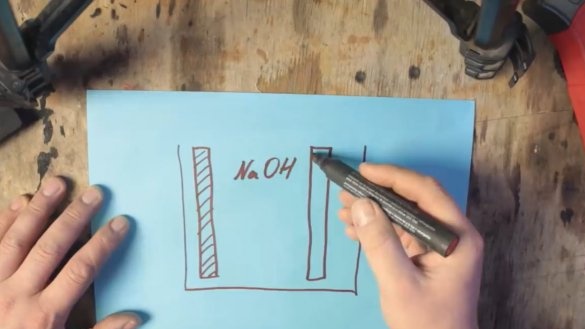
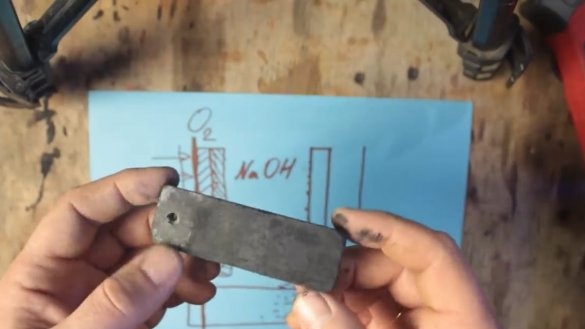
Damit eine solche Batterie funktioniert, werden zwei Elektroden benötigt: eine natürlich aus Aluminium und die zweite aus Graphit. Beide Elektroden befinden sich in einer Elektrolytlösung.
Salz (NaCl) kann als Elektrolyt verwendet werden, aber damit können Sie die Spannung auf etwa 0,7 V erhöhen. Die Spannung des alkalischen Elektrolyten (NaOH) kann bereits weiter auf etwa 1 V erhöht werden.
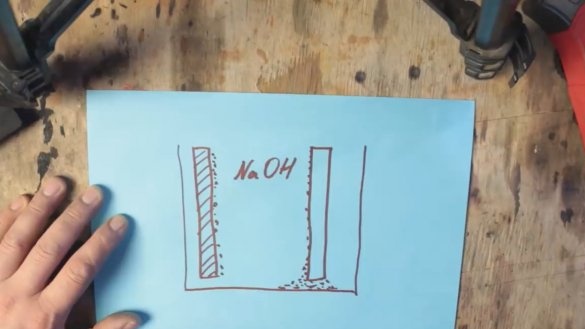
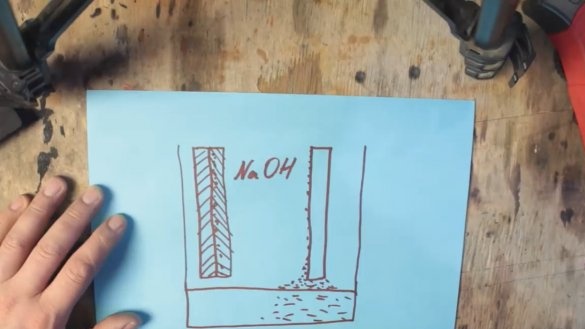
Während der chemischen Reaktion wird Aluminium mit einer Schicht aus Aluminiumhydroxid (Al (OH) 3) beschichtet, die allmählich auf den Boden des Tanks sinkt. Und auf der Oberfläche der Graphitelektrode bilden sich Wasserstoffblasen, die wiederum zu einer Erhöhung des Widerstands und einem Spannungsabfall führen. Dieser Vorgang wird als Polarisation bezeichnet.
Das erste Problem bei der Ausfällung von Aluminiumhydroxid kann durch einfaches Erhöhen der Kapazität, in der sich das verbrauchte Produkt absetzt, beseitigt werden. Das zweite Problem kann jedoch durch eine depolarisierende Masse auf Manganoxidbasis behoben werden, die sich während des Betriebs in Manganhydroxid verwandelt.
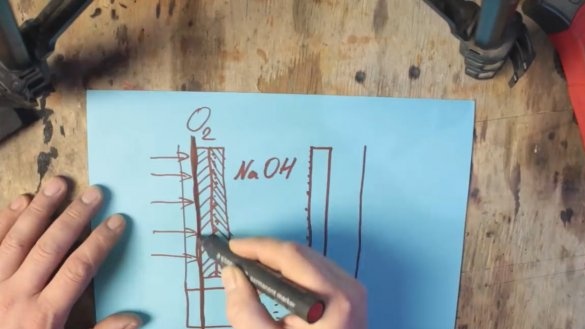
Tatsächlich haben wir eine gewöhnliche Alkalibatterie, aber nur eine sehr große. Es entsteht jedoch ein neues Problem. Tatsache ist, dass Manganoxid ebenfalls verbraucht wird und auch geändert werden muss. Und wir müssen sicherstellen, dass nur Aluminium ausgegeben wird. Nehmen Sie dazu Sauerstoff aus der Umgebungsluft. Hier beginnt die Aluminium-Luft-Batterie. Eine der Wände muss nur durch eine gasdurchlässige Membran ersetzt werden, und die Graphitelektrode muss durch eine Mischung aus Graphit und Manganoxid mit Platin- oder Silbernanopartikeln ersetzt werden.
Manganoxid mit Edelmetallnanopartikeln reagiert nicht, sondern wirkt als Katalysator, wodurch Wasserstoff aus dem Elektrolyten durch Luftsauerstoff oxidiert wird.
Die Technologie zur Herstellung von Manganoxid mit Einschlüssen von Silbernanopartikeln ist im Prinzip nicht kompliziert und kann unter handwerklichen Bedingungen ausprobiert werden. In diesem Artikel wird jedoch erläutert, wie Sie die kostengünstigste Option für eine Batterie auswählen können, die Energie aus Aluminium erhält. Die folgenden Anweisungen stammen vom Fiery TV-Kanal YouTube. Ausführlicher im Originalvideo des Autors:
Die Version mit maximalem Budget für Graphit sind Sommerkontakteinsätze für Oberleitungsbusse. Sie können sie absolut kostenlos an den letzten Obushaltestellen finden, oder Sie können sie kaufen, sie sind nicht teuer, der Autor fand sie zum Verkauf bei 22 Rubel pro Stück.
Als nächstes brauchen wir ein Alkali. Hier ist ein Werkzeug zum Reinigen von Rohren in seiner Zusammensetzung enthält hundertprozentig Natriumalkali.
Um die Alkalireaktion zu starten, benötigen wir nur ein wenig, 1 g Alkali pro 0,5 l Wasser reicht aus.
Lassen Sie uns zunächst prüfen, ob in dieser Batterie wirklich eine Graphitelektrode benötigt wird. Nehmen wir zur Erfahrung diese Edelstahlelektrode.
Jetzt setzen wir die Aluminiumplatte und die Edelstahlelektrode in das Alkali ein, schließen das Multimeter an und sehen, wie viele Volt sich herausstellen.
Wie Sie sehen können, stellte sich heraus, dass es ungefähr 1,4 V waren. Überprüfen wir nun den Kurzschlussstrom.
Kurzschlussstrom im Bereich von 20mA. Welche Schlussfolgerungen können gezogen werden: Theoretisch ist es unter extremen Bedingungen möglich, eine Batterie aus Edelstahlbechern und Aluminiumfolie zusammenzubauen.
Als nächstes werden wir eine Kupferelektrode aus elektrischem Kupfer haben.
Wie wir beobachten können, stellte sich heraus, dass die Spannung etwas höher als 1,4 V war, aber der Kurzschlussstrom war zuerst hoch, aber dann begann er ziemlich schnell durchzuhängen und das Kupfer begann auch mit einer dunklen Beschichtung bedeckt zu werden, höchstwahrscheinlich wurde dieser Effekt durch Verunreinigungen im Wasser verursacht, da In diesem Experiment nahm der Autor einen Tipp von einem Tipp.
Tauchen Sie nun die Graphitelektrode in die Elektrolytlösung.
Mit dieser Elektrode wurde eine Spannung von 1,3 V erhalten, wobei der Kurzschlussstrom im Bereich von 17 mA gestoppt wurde. Auf den ersten Blick scheint die Edelstahlelektrode effizienter zu sein, aber die Oberfläche der Edelstahlelektrode ist größer, so dass noch nicht bekannt ist, welcher Graphit oder Edelstahl besser ist.
Da Graphit eine ziemlich große Beständigkeit hat, müssen Sie irgendwie damit umgehen. Es ist notwendig, Elektroden aus einem gut leitenden Material herzustellen, und Graphit sollte sich nur auf seiner Oberfläche befinden.Es wurde beschlossen, durch den Graphit zu bohren und in die resultierenden Löcher das Gewinde für die m6-Schrauben zu schneiden.
Das Ergebnis ist eine Stahlelektrode mit einer Graphithülle.
Der Widerstand von nicht gebohrtem Graphit beträgt etwa 4,5 Ohm, von gebohrtem Graphit jedoch etwa 1,7 Ohm.
Im Gesicht nimmt eine Abnahme des Widerstands und folglich die Wirksamkeit der Struktur zu. In weiteren Experimenten werden wir destilliertes Wasser verwenden.
Das erste Experiment mit einem Elektrolyten, bei dem 4 g Alkali pro 1 Liter Wasser.
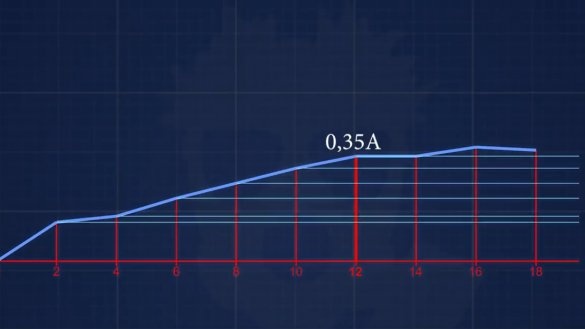
Kurzschlussstrom stellte sich heraus 150mA. Der nächste Elektrolyt hat eine Konzentration von 6 g Alkali pro 1 Liter. Nun und so weiter, jedes Mal erhöhen wir die Konzentration um 2 g, bis wir eine Konzentration erreichen, bei der der Strom nicht ansteigt.
Obwohl eine solche einfache Batterie keinen großen Stromwirkungsgrad aufweist, kann eine solche Batterie sehr lange arbeiten, und jedes Aluminium kann als Elektrode verwendet werden, die leicht zu Elektroden jeder Form geschmolzen werden kann, beispielsweise Aluminiumdosen verschiedene alkoholische und alkoholfreie Getränke, Schokoladenfolie usw.
Als Ergebnis wird nach all den Experimenten mit unterschiedlichen Elektrolytkonzentrationen klar, dass es bei dieser Konstruktion der Batterie keinen Sinn macht, mehr als 12 g Alkali zu 1 Liter Wasser zu geben, dh wir erhalten ungefähr 1% ige Lösung.
Dann stellte der Autor einen weiteren Clip zusammen, der aus 3 Elektroden bestand.
Zwei Batterien ergeben eine höhere Spannung und weniger Verluste, sodass das Ergebnis besser ist.
Nehmen wir nun einen Eimer Elektrolyt, ein großes Stück Aluminium und 2 Edelstahlelektroden.
In einem Eimer eine Elektrolytkonzentration von 10 g / 1 l. Spitzenstrom 1,3A, sackte es auf 520mA. Bei all der großen Fläche aus rostfreiem Stahl war es nicht mit Graphit zu vergleichen, da sich herausstellte, dass es mit Graphit 600 mA betrug. Übrigens wird bei der Reaktion Wasserstoff freigesetzt, der auch gesammelt und als Energiequelle genutzt werden kann. Kurz gesagt, es gibt Raum zum Wachsen. Das ist alles für jetzt. Danke für die Aufmerksamkeit. Bis bald!